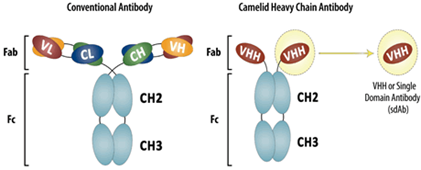
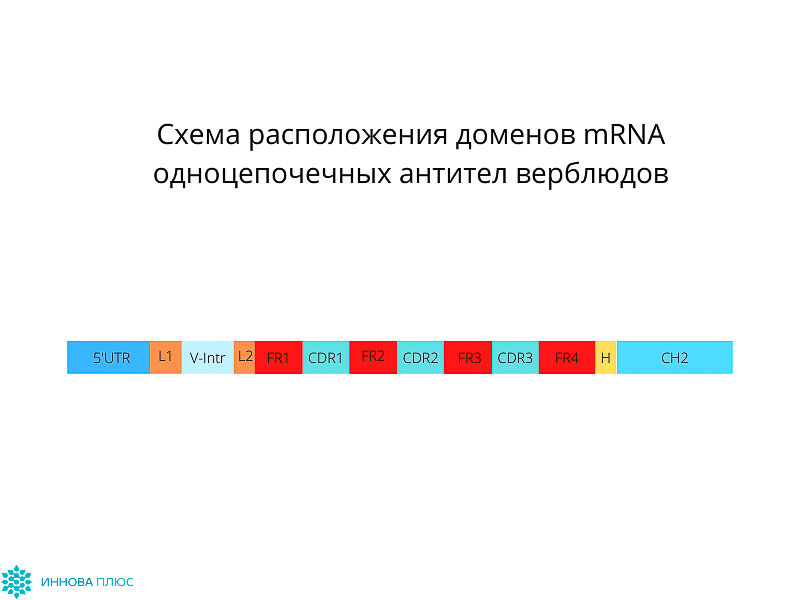
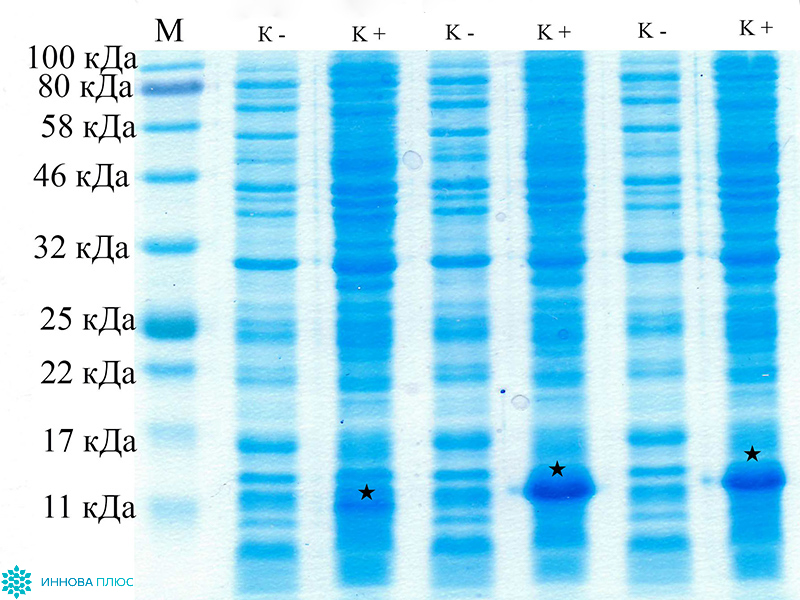
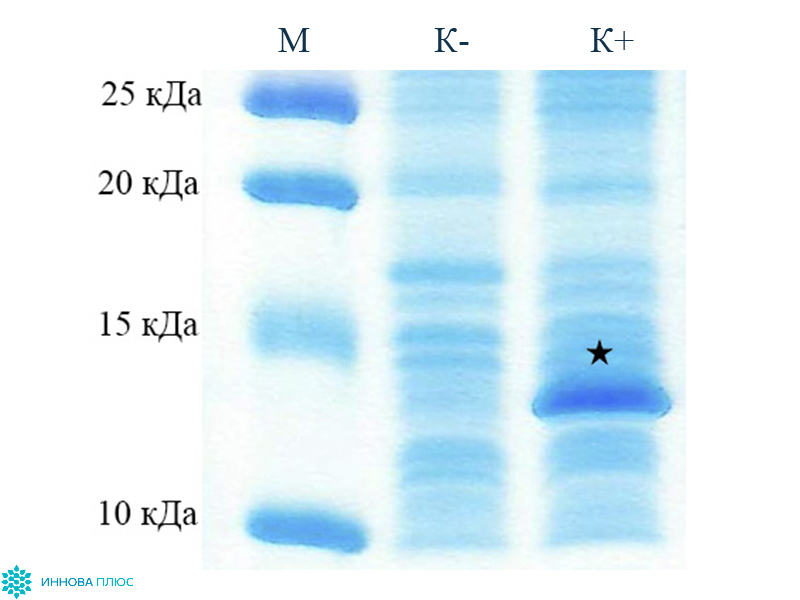
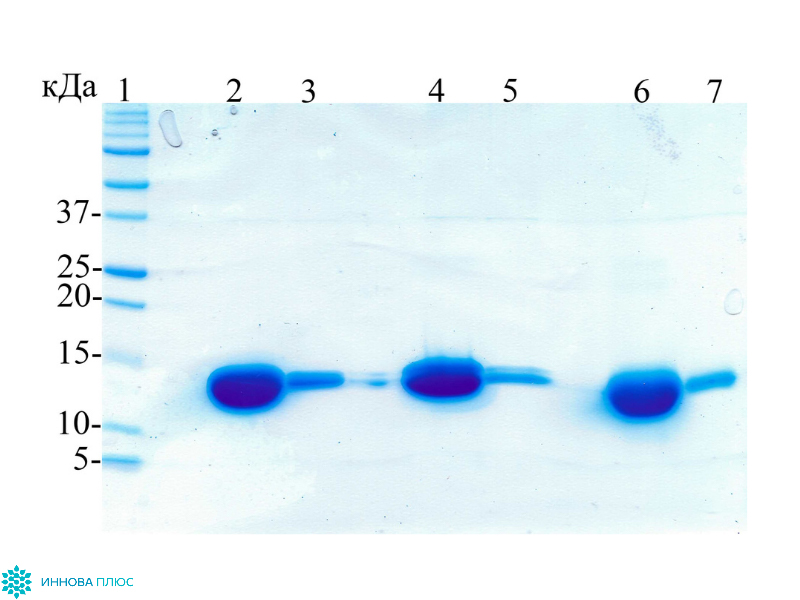
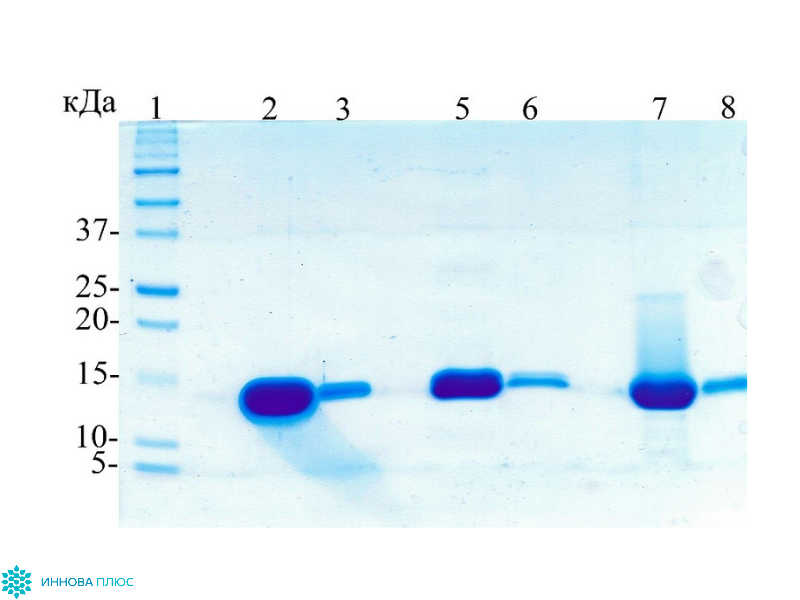
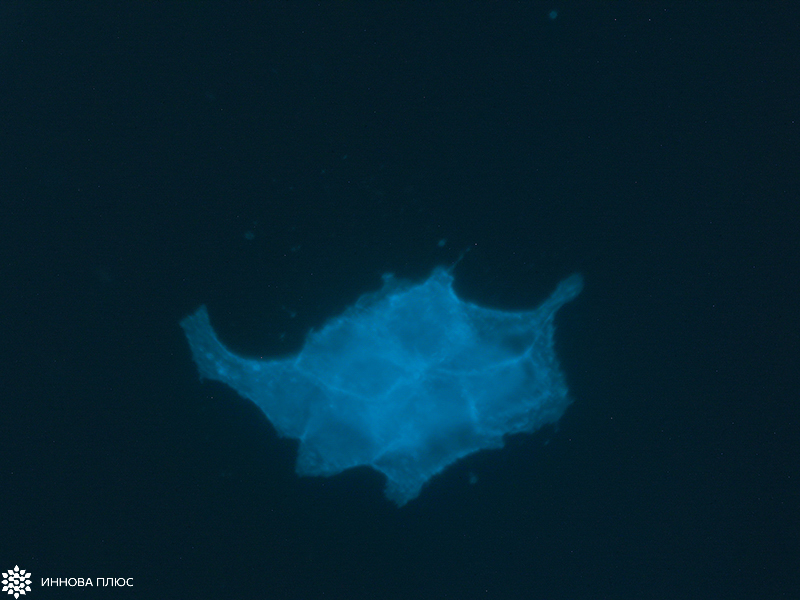
У представителей семейства Верблюдовых (верблюдов, лам, альпак) и у надотряда Акул случайно были обнаружены одноцепочечные антитела, содержащие только тяжелые цепи. Вариабельная область этих антител состоит всего из одного домена размером 13-15 кДа (single-domain antibody, sdAb) и проявляет все свойства классических полноразмерных антител класса IgG. Благодаря небольшому размеру, высокой гидрофильности и термической стабильности наноантител, они с высокой эффективностью воспроизводятся в клетках бактерий E. coli. Отобрав нужный нам вариант sdAb из иммунизированного верблюда Camelus dromedarium (Верблюд двугорбый) или акулы Scyliorhinus canicula (Кошачья акула обыкновенная), мы производим VHH и VNAR фрагменты антител методом фагового дисплея с последующим биопеннингом.